崇雨田主任:乙型肝炎的预防
传染病的流行过程包括传染源、传播途径和易感人群三个环节,针对这三个环节采取综合性措施,并根据不同传染病的特点,预防措施的侧重点各有不同。对乙型肝炎而言,对于易感人群的免疫预防是最重要的预防措施,如随着乙型肝炎疫苗的广泛应用,我国的乙型肝炎流行态势已初步得到控制。
现将乙型肝炎预防的三个要点分述如下:
一、管理传染源
1.传染源
人类感染HBV后可以表现为急性期患者、慢性期患者、携带者等多种形式,由于携带者、慢性期患者携带HBV时间长、隐蔽而且人数多,因此具有重要的公共卫生意义,同时也决定了乙型肝炎的传染源管理具有难度大的特点。理论上,对HBV感染者实施抗病毒治疗,有助于减少感染者的传染性,但鉴于目前抗病毒治疗手段存在局限,并不主张为降低传染性而广泛使用抗病毒治疗。
2.疫情报告
乙型肝炎属于乙类传染病,应根据国家有关法律法规要求,执行疫情报告制度。
3.特殊职业人群的管理
如幼儿园工作人员,应加强从业人员的入职前体检,如为HBV感染者应避免从事幼师工作。由于幼儿相处一起时相互间常常厮打,有可能导致皮肤破损、出血,因此幼儿入托前可进行筛查,但中小学生入学时不应拒收HBV感染者。虽然,可以从唾液、泪液等体液中分离到少量HBV,但共餐、共用厕具等行为未被证实可以传播乙型肝炎。因此,除国家规定的情况外,不得以HBV携带为理由拒收应聘者。对筛查发现的HBV感染者应加强健康教育,使其掌握防止疾病传播的知识。
二、切断传播途径
1.切断经血制品传播
推行无偿献血,加强血制品筛查;长期接受血制品治疗的患者,如血友病、血液透析患者等,应接受乙型肝炎疫苗接种。
2.防止医院感染
HBV感染者需接受血液隔离;推广一次性医疗器材,对重复使用的医疗器械应严格灭菌;医护人员应严格执行标准预防制度。有效的灭活HBV的方法包括:环氧乙烷、过氧乙酸、强化戊二醛、漂白粉、碘伏等,或者γ射线照射,或者高温高压蒸汽灭菌。过去常用HBsAg的破坏代表HBV灭活,实际上HBV感染性消失常早于HBsAg的破坏。
3.阻断性接触传播
加强宣传教育,普及性知识,取缔性交易,鼓励安全的性行为。对HBV感染者的配偶应进行乙型肝炎疫苗接种。
4.切断母婴传播
乙型肝炎的母婴多为分娩时接触母体血液或体液,因此,妊娠期间尽量避免羊膜腔穿刺,缩短分娩时间,保持胎盘完整性,尽量减少暴露于母血的时间。新生儿出生后实施紧急免疫程序。虽然有研究提示妊娠末期孕母接受乙型肝炎免疫球蛋白(HBIg)注射或者联合拉米夫定有助于进一步减少母婴传播几率,但由于目前采用的新生儿免疫程序已能有效阻断近90%的母婴传播,再加上孕母接受HBIg注射或者联合拉米夫定需要承担较大的风险,因此,我们认为在缺乏足够循证医学依据之前,不宜推广妊娠末期孕母肌内注射HBIg或者联合口服拉米夫定。
5.注意日常生活的细节
日常生活和工作中的一般接触并不会传播乙型肝炎,但有一些小细节仍需注意。例如,不要混用剃刀、牙刷,不接受未经消毒的文身、穿耳、修足,女性感染者在月经期应小心处理内裤、卫生巾等。
三、保护易感人群
(一)乙型肝炎的保护性免疫机制
针对HBV的保护性抗体是抗-HBs,它可以中和细胞外的HBV,阻止其感染细胞;另有研究显示,IgG型的抗-HBs可以经FcRn介导的胞吞作用进入肝细胞内,推测抗-HBs的胞内作用可能有助于在感染早期控制感染扩散。此外,抗-PreS1和抗-PreS2也有保护作用,且通常比抗-HBs更早产生;抗-HBe和抗-HBc不具有直接的保护作用,但在动物试验中表现出协同清除病毒的能力。由于HBsAg具有共同抗原决定簇a,因此不同血清亚型的HBV之间具有很高的交叉保护性。自然感染HBV的恢复期患者,以及通过注射疫苗获得免疫力的人,其抗-HBs均以IgG1型为主。HBsAg是胸腺依赖性抗原,但HBsAg特异的B细胞的激活却不受MHC限制。例如,PreS抗原特异的T细胞,不仅能辅助PreS抗原特异的B细胞,亦能辅助HBsAg特异的B细胞。机体对HBsAg的应答性与不同的MHC表现型有关,有些人“天生”就对HBsAg为主要成分的疫苗反应差,但在自然感染后仍能清除病毒,并产生高滴度的抗-HBs,这可能就是因为PreS抗原特异T细胞辅助激活HBsAg特异的B细胞。由于HBV在复制过程中存在反转录经过,突变率较高,感染者体内可存在多个亚种,可以预见,如果施以抗-HBs的选择压力,有可能选择出不与抗-HBs结合的HBsAg变异株,称为HBsAg免疫逃逸株。清除细胞内的HBV,主要依靠细胞免疫。HBV感染的自然史说明,健全的细胞免疫有助于感染的局限化,并对最终清除HBV起决定性作用。理论上讲,注射乙型肝炎疫苗后,尤其是注射含有特殊佐剂的疫苗后,应能激活HBV特异性细胞免疫,但临床上尚无实用的方法测定个体的特异性细胞免疫。另外,PreS抗原与S抗原(HBsAg)的应答性不一定平行,T细胞的激活性能上,通常PreS抗原比S抗原更优异。
(二)易感人群
对HBV缺乏特异性免疫者易感。针对HBV的体液免疫和细胞免疫均有预防作用,但通常采用抗-HBs滴度标定个体对HBV的特异性免疫力。一般认为,抗-HBs<10mIU/ml者均为易感人群。目前,HBsAg免疫逃逸株尚属散发流行,但是仍应警惕疫苗失效的潜在威胁。值得注意的是,免疫低下人群即使存在足够滴度的抗-HBs,亦可能对HBV易感。韩国学者Kim等报道了多例抗-HBs阳性肾移植受体术后出现HBV感染,分离毒株进行基因分析,发现有野生株感染的证据,因此,该作者认为在乙型肝炎高流行区,应该重新评价抗-HBs对器官移植受体的保护作用。这一研究也提示,在乙型肝炎的保护性免疫中,健全的细胞免疫可能是不可或缺的一环。肾移植术的受体,由于长期服用抑制细胞免疫的药物,即使体液免疫正常(足够滴度的抗-HBs),对HBV也可能易感。
(三)高危人群
HBV感染母亲所产的新生儿、HBV感染者的家属、医护人员、军警、需长期大剂量接受血制品者(如血友病患者、长期血液透析患者)、静脉药瘾者、多个性伴侣者、性病患者、服刑人员等。鉴于免疫低下者感染HBV后容易慢性化,建议接受乙型肝炎疫苗接种,这些人包括HIV感染者、计划实施化疗或放疗者、等待移植的受体等。
(四)人工主动免疫
我国的乙型肝炎疫苗研制工作始于20世纪70年代末,1986年第一株国产的血源疫苗问世,2001年后血源疫苗基本上被基因工程重组疫苗取代。1992年,卫生部推荐乙型肝炎疫苗常规用于婴儿的免疫接种,但这一建议不具有强制力,且疫苗及其接种费用需由家长负担,因此各地实施并不均衡。自2002年起,卫生部将乙型肝炎疫苗列入计划免疫,免费为新生儿提供疫苗,但家长仍需支付接种费。2005年起,卫生部在全国范围内提供全免费的乙型肝炎疫苗接种服务。2006年统计,10岁以下儿童的慢性HBV携带率已从10%下降到1%~2%,总人群的HBV携带率也下降了2.8%。由此可见,乙型肝炎预防的最主要措施是乙型肝炎疫苗。
1.血源疫苗
人类对乙型肝炎疫苗的研究始于1971年,美国默克药厂研发的疫苗是最早获准生产的疫苗。它利用慢性HBV感染者体内存在大量“空壳”病毒的特性,从慢性HBV携带者的血浆中离心、提纯HBsAg颗粒,然后采用胃蛋白酶、尿素、甲醛三步法化学灭活可能混入的感染性颗粒,最后加上佐剂制备而成。因其来源于人的血浆,故称为血源疫苗。这是第一代的乙型肝炎疫苗,最大的优点在于免疫原结构最接近天然状态,接种效果良好。但是,从感染者的血液获取免疫原并不是制备疫苗的常规途径,随着接种范围的扩大,会最终丧失免疫原的来源。另外,血源疫苗存在一定的安全隐患,有可能导致未知的血液传播疾病的流行。因此,目前已将血源疫苗淘汰。
2.基因工程重组疫苗
将负责编码HBsAg的S基因通过基因工程的方法引入合适的表达系统中,经发酵或细胞培养后收集细胞,再经碾碎、抽提、层析等工艺后得到纯化的HBsAg,加入佐剂及防腐剂即制成成品疫苗。目前采用的表达系统通常是酵母细胞,亦有选取动物细胞的,如中国仓鼠卵巢细胞(简称CHO细胞)。由于不同宿主细胞之间的翻译后修饰系统有所差异,不同的表达系统产生的HBsAg之间的结构并不一致,并且和人体细胞表达的HBsAg相比也略有差异,主要表现在不同的蛋白质分子糖化方式。因此,从接种效果上看,基因工程重组疫苗略逊于血源疫苗。各种血清型的S基因所制备的疫苗均能刺激机体产生抗a决定簇的抗体,因此,对其他血清型的HBV均有交叉免疫性。可以采用肌内注射或皮下注射的方式进行接种,因为皮下注射比较疼痛,且容纳的注射量小,所以常规使用肌内注射。新生儿选择的部位是大腿前部外侧的肌肉,儿童、青少年及成人则在三角肌。基因工程重组疫苗安全性优良,除偶有低热、注射部位疼痛、过敏外,无明确的重大不良反应,而且孕妇、新生儿、免疫缺陷人群、HBV感染者均可接受注射。由于本疫苗安全、有效、稳定,是目前临床最常用的乙型肝炎疫苗。
3.含PreS抗原的基因工程重组疫苗
以HBsAg为免疫原的疫苗有三大缺陷:①存在弱应答甚至无应答人群,尤其是需要积极保护的血液透析患者;②应答缓慢,按“0-1-6”方案接种后,需在第6个月以后抗-HBs水平才能达到高峰;③对免疫逃逸株无效。针对这些问题,研发了PreS+HBsAg的联合疫苗。如前文所述,PreS抗原的应答调节机制与HBsAg不同,因此,HBsAg弱应答或无应答人群仍有可能对PreS抗原强应答。与此同时,PreS抗原还是良好的T细胞抗原,而且致敏的T细胞还能交叉辅助HBsAg特异B细胞应答,提高HBsAg应答率。另外,抗-PreS也是保护性抗体,同样可以提供保护,更重要的是,这种保护还能涵盖a决定簇变异导致的免疫逃逸株。鉴于PreS+HBsAg联合疫苗能更快地刺激机体产生保护性抗体,也有人认为更适合于高危新生儿的接种,提高母婴传播的阻断率。虽有多种优点,但本类疫苗尚待积累更多的临床数据和经验,暂未广泛应用。
4.联合疫苗
由于乙型肝炎疫苗与白百破、麻疹等疫苗联用无拮抗作用,且小儿计划免疫的疫苗种类增加需通过简化免疫程序达到提高覆盖率的目的,已有多种联合疫苗通过临床验证获准上市。其中,临床常用的是甲型肝炎+乙型肝炎联合疫苗。这些联合疫苗中的乙型肝炎疫苗组分,仍为HBsAg基因工程重组疫苗,不含PreS抗原。
(五)人工被动免疫
1.免疫球蛋白
免疫球蛋白提取自一般的血源,其抗-HBs滴度常不足1∶50,且波动较大。随着普种乙型肝炎疫苗人群的增加,免疫球蛋白的抗-HBs滴度可能因此增加,但在目前,上市的免疫球蛋白无法满足预防HBV感染的需要,因此,仍应采用效价高且稳定的乙型肝炎免疫球蛋白(HBIg)。
2.乙型肝炎免疫球蛋白(HBIg)
血源为乙型肝炎疫苗免疫的健康人群,经低温乙醇法提取血浆中的免疫球蛋白,其抗-HBs滴度高达1∶200000(200IU/ml),肌注后半衰期平均为(24.0±3.8)天。
(六)人工主动免疫方案
1.暴露前预防方案
(1)在各种不同的免疫方案中,按“0-1-6”方案接种产生的抗-HBs水平最高。因此,针对不同人群的疫苗接种方案基本上采用“0-1-6”方案,区别仅仅是疫苗的剂量不同,归纳入表1。
表1 不同人群的疫苗接种方案
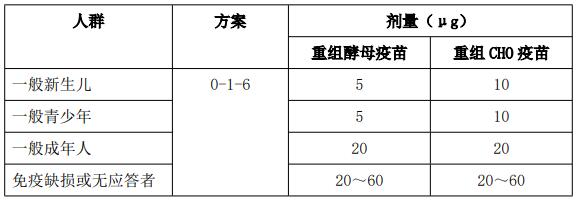
(2)效果评价:完成乙型肝炎疫苗接种程序后可以检查抗-HBs滴度以评价免疫效果。一般认为有抗体应答者保护期可维持至少12年,通常无需检测抗-HBs或行加强免疫。对高危人群则应监测抗-HBs滴度,在小于10mIU/ml时应行加强免疫。
(3)无应答/弱应答人群:有5%~10%的人对HBsAg基因工程重组疫苗无应答/弱应答。已知的无应答/弱应答高危因素包括HBsAg阳性母亲所产子女、高龄、早产、酗酒、嗜烟、肥胖、血液病、慢性肾衰竭接受血液透析、HIV感染等。由于测定抗体水平远比测定细胞免疫水平容易,因此,“无应答/弱应答”这个术语针对的是体液免疫。体液免疫应答差,并不代表细胞免疫应答弱,因此,完全有理由相信在上述人群中,尤其是其中的健康人,可能已经借助细胞免疫获得对HBV的特异性免疫力。
(4)无应答/弱应答的补救方案:国内近半数无应答/弱应答成人实际上已有隐匿性HBV感染,因此,在排除接种者为隐匿性感染者之后,由于HBsAg基因工程重组疫苗的安全性良好,可以优先考虑更高的接种剂量,如60μg。其次,可以考虑更换疫苗的品牌,例如,重组酵母疫苗无效者,可考虑换用重组CHO疫苗。因为不同的表达系统产生的HBsAg其糖化结构不同,有可能打破宿主的无反应性。更换接种方式也可改善应答,皮肤含有丰富的抗原提呈细胞,若接种者应答差,改用皮下注射有助于提高应答率。换用“0-1-2-6”或“0-1-6-12”接种方案略有帮助,但抗-HBs阳性率、滴度和持续时间仍欠满意。改良佐剂,或者加用小剂量IFN、IL-1、GM-CSF对免疫低下人群可能有用。前文已述,改用含PreS抗原的基因工程重组疫苗能有效提高应答率,但此类疫苗目前尚未大规模应用于临床。业已证明,HAV+HBV联合疫苗也有类似效果,其机制可能也是借助HAV致敏的T细胞交叉辅助HBsAg特异B细胞应答。在临床工作中,还需要向无应答/弱应答者做好解释工作:对疫苗反应差,不代表身体不能自行清除HBV,也不代表免疫系统存在毛病;另外,随着乙型肝炎免疫人群的扩增,形成的人群免疫屏障能阻断HBV的人传人,间接达到保护无应答/弱应答者的目的;如果意外暴露于HBV,也可借助乙型肝炎免疫球蛋白进行预防。
2.暴露后预防方案
(1)HBV感染孕妇所产新生儿:已经证实有效的方法是出生后尽早(<12小时)注射乙型肝炎免疫球蛋白至少100IU,同时在另一个部位注射乙型肝炎疫苗(10μg重组酵母疫苗,或20μg重组CHO疫苗),此后在第1个月、第6个月再次接种乙型肝炎疫苗(10μg重组酵母疫苗,或20μg重组CHO疫苗)。经此处理的新生儿,可安全接受母乳喂养。妊娠期间使用乙型肝炎免疫球蛋白和/或拉米夫定,降低母婴传播的作用有限,同时会带来应用血制品和/或核苷类似物的风险,一般不推荐使用。
(2)成人意外暴露后:首先,根据暴露部位的特点选择能杀灭的HBV的消毒剂进行伤口处理。然后,根据抗-HBs的情况确定下一步方案:①抗-HBs≥10mIU/ml者,无需特殊处理;②抗-HBs<10mIU/ml或不详者,肌注乙型肝炎免疫球蛋白200~400IU,同时在另一个部位注射乙型肝炎疫苗(20μg重组酵母疫苗),此后在第1个月、第6个月再次接种乙型肝炎疫苗(20μg重组酵母疫苗)。同时,监测HBV血清学标志物及肝功能。
(3)免疫逃逸株暴露后预防:目前免疫逃逸株并未呈现大规模流行态势,但高危人群,尤其是医护人员仍有可能暴露于免疫逃逸株。针对野生株的重组乙型肝炎疫苗及乙型肝炎免疫球蛋白并没有作用,因此,暴露于可疑/确定免疫逃逸株后可考虑改用含PreS抗原的基因工程重组疫苗及核苷(酸)类似物进行紧急预防。
(七)特殊的临床问题——预防肝移植术后供肝再感染
争取在肝移植术前1~3个月开始核苷(酸)类似物抗病毒治疗,减少病毒载量;术中无肝期加用乙型肝炎免疫球蛋白;术后长期使用核苷(酸)类似物和小剂量乙型肝炎免疫球蛋白。研究及争议较多的是术后乙型肝炎免疫球蛋白的剂量和疗程。即使按上述流程执行,供肝仍有再感染风险,主要的威胁是免疫逃逸株和核苷(酸)类似物耐药株。
参考文献
[1] 骆抗先.乙型肝炎基础和临床. 3版.北京:人民卫生出版社,2007.
[2] 田庚善. 病毒性肝炎// 王季午. 传染病学. 3版. 上海:上海科学技术出版社,1998.
[3] 彭文伟. 病毒性肝炎研究. 广州:广东科技出版社,1998.
[4] 彭文伟. 传染病学. 6版. 北京:人民卫生出版社,2004.
[5] 中华医学会肝脏病学分会,中华医学会感染病学分会.慢性乙型肝炎防治指南. 中华肝脏病杂志, 2005,13(12):881-891.
[6] Cardell K, Akerlind B, Sällberg M, et al. Excellent response rate to a double dose of the combined hepatitis A and B vaccine in previous nonresponders to hepatitis B vaccine. J Infect Dis, 2008,198(3): 299-304.
[7] LuoKX, Wang LP, Nie J, et al. Is nonresponsiveness to hepatitis B vaccine due to latent hepatitis B virus infection? J Infect Dis,1992, 165(4):777-778.
[8] King JW, Taylor EM, Crow SD, et al. Comparison of the immunogenicity of hepatitis B vaccine administered intradermally and intramuscularly. Rev Infect Dis,1990,12(6):1035-1043.
[9] Rimola A, García-Tsao G, Navasa M, et al. Diagnosis, treatment and prophylaxis of spontaneous bacterial peritonitis: a consensus document. J Hepatol, 2000, 32(1): 142-153.
[10] Sechser A, Osorio J, Freise C, et al. Artificial liver support devices for fulminated liver failure. Clin Liver Dis,2001,5(2):415-424.
[11] 中华医学会传染病与寄生虫病学分会、肝病学分会. 病毒性肝炎防治方案. 中华肝病杂志, 2000,8:324-329.
[12] 张赤志,田德英. 中西医结合肝脏病学. 北京:人民军医出版社,2002.
[13] Schrier RW, Arroyo V, Bemardi M, et al. Peripheral arterial vasodilation hypothes is proposal for the initiation of renal sodium and water retention in cirrhosis. Hepatology, 1988, 8(5): 1151-1157.
[14] Gines P, Guevara M, Arroyo V, et al.Hepatorenal syndrome. Lancet, 2003, 362: 1819-1827.
[15] Moreau R, Durand F, Poynard T. et al. Terlipressin in patients with cirrhosis and type Ⅰhepatorenal syndrome: a retrospective multicenter study. Gastroenterology, 2002, 123(6): 2160-2161.
[16] Haliml C, Bonnard P, Bernard B, et al. Effect of terlipressin on hepatorenal syndrome in cirrhotic patients: results of a multicentre pilot study. Eur J GastroenterolHepatol, 2002, 14: 153-158.
[17] Alessandrial C, Venon WD, Marzano A, et al. Renal failure in cirrhotic patients: role of terlipressin in clinical approach to hepatorenal syndrome type 2. Eur J GastroenterolHepatol, 2002, 14: 1363-1368.
[18] Colle I, Durand F, Pessione F, et al. Clinical courses, predicitive factors and prognosis in patients with cirrhosis and type Ⅰhepatorenal syndrome treated with terlipressin: a retrospective ananlysis. J GastroenterolHepatol, 2002, 17: 882-888.
[19] Solanki P, Chawla A, Garg R, et al. Beneficial effects of terlipressin in hepatorenal syndrome: A prospective, randomized placebo-controlled clinical trial. J GastroenterolHepatol, 2003, 18: 152-156.
[20] 许德军,王晓伟,徐嘉. 乙型肝炎病毒e抗原阴性慢性乙型肝炎患者的肝组织病理分级分期及其与丙氨酸氨基转移酶的关系. 临床内科杂志, 2007,24(2):94-95.
[21] 张婷杰. 乙型肝炎患者血清自身抗体检测的临床讨论. 内蒙古医学杂志, 2005,37(11):1020-1021.
[22] Patel K, Gordon SC, Jacobson I, et al. Evaluation of a panel of non-invasive serum markers to differentiate mild from moderate to advanced liver fibrosis in chronic hepatitis C patients. J Hepatol, 2004, 41(6): 935-942.
[23] 危北海,张万岱,陈治水,等. 肝硬化中西医结合诊治方案(草案).中国中西医结合杂志, 2004,24(10):869-871.
[24] 郭琳琅,郭颖,肖莎. 凋亡基因bcl-2、bax及Faxs在肝硬化中的表达及与乙肝病毒感染的关系. 临床肝胆病杂志, 1999,15(1):30-31.
[25] Gerlach J. Hybrid liver support. Int JAnd Organs,1996,19(1):1-2.
[26] 中华医学会肝脏病学分会,中华医学会感染病学分会. 慢性乙型肝炎防治指南(2010年版).中华肝脏病杂志, 2011,19(1):13-21.

崇雨田
主任医师、博士生导师,现任中山大学附属第三医院副院长。广东医师协会感染病学分会主任委员,广东省肝脏病学会肝炎专业委员会名誉主任委员,广东省干部保健专家。多年来的工作重点为终末期肝病尤其肝衰竭的内科综合治疗研究及慢性乙型肝炎的抗病毒治疗药物的临床系列研究工作,在重型病毒性肝炎、肝衰竭病例的抢救治疗、慢性病毒性肝炎抗病毒治疗等方面有丰富经验。
来源:人民卫生出版社《临床知识》约稿
作者:崇雨田主任医师,中山大学附属第三医院副院长;吴昊
编辑:环球医学资讯丁好奇
- 评价此内容
- 我要打分
近期推荐
热门关键词
合作伙伴
Copyright g-medon.com All Rights Reserved 环球医学资讯 未经授权请勿转载!
网络实名:环球医学:京ICP备08004413号-2
关于我们|
我们的服务|版权及责任声明|联系我们
互联网药品信息服务资格证书(京)-经营性-2017-0027
互联网医疗保健信息服务复核同意书 京卫计网审[2015]第0344号
 会员登录
会员登录

