一例肺泡蛋白沉积症的诊治经验分享
51岁男性,因咳嗽8个月,胸闷伴气促1个月入院。如何诊治?
一、入院疑诊
(一)病例信息
【病史】
男性患者,51岁,因咳嗽8个月,胸闷伴气促1个月入院。患者于8个月前,感冒后开始出现咳嗽,偶有咳痰,痰为黑色、量少,无畏寒、发热、胸痛、胸闷、咯血、恶心、呕吐等不适,未进行特殊治疗,后间断有咳嗽、咳痰症状,痰仍为黑色,近1个月来,症状加重,以干咳为主,伴胸闷、气促,活动后加重,无夜间端坐呼吸,无畏寒、发热,无咯血,无恶心、呕吐等不适。患者于当地医院就诊,胸部CT提示双肺弥漫性病变、右下肺团块影,对症治疗(具体不详)后复查胸部CT示肺部病灶无吸收。我院门诊以“肺弥漫性间质性病变、肺部感染”收入院。患者自发病以来,精神、食欲一般,大小便正常,体力有下降,体重无明显变化。
5年前患者曾在煤矿工作4个月,平素身体状况良好;否认肝炎、结核等传染病病史,否认高血压、心脑血管疾病、糖尿病及精神病病史,有腰椎间盘突出病史;否认食物、药物过敏史;否认外伤、手术、输血史。
【体格检查】
体温37.9℃,心率88次/min,呼吸22次/min,血压120/80mmHg;SpO2 88%(未吸氧);神志清楚,精神差,口唇发绀;颈软,气管居中,颈部浅表淋巴结未触及肿大;双肺呼吸音粗,双下肺可闻较多湿啰音;心律齐,未闻病理性杂音;腹软,无压痛及反跳痛,肝、脾肋下未触及;双下肢不肿。
【影像学检查】
外院胸部CT检查提示双肺弥漫性病变,右下肺团块影。
(二)临床思辨
【临床特点】
1.患者为中年男性,病程呈慢性。
2.主要症状为咳嗽8个月,胸闷伴气促1个月。
3.体温37.9℃,SpO2 88%(未吸氧);神志清楚,精神差,口唇发绀,双肺呼吸音粗,双下肺可闻较多湿啰音。
4.胸部CT检查提示双肺弥漫性病变,右下肺团块影。
5.抗感染治疗效果不佳。
【思辨要点】
咳嗽、咳痰、胸痛、呼吸困难、肺内湿性啰音或哮鸣音是肺部疾病的常见症状和体征,无病因特异性,许多原因均可表现为同样的症状和体征。本例患者胸部影像学表现为双肺弥漫性病变,可以此为出发点进行鉴别诊断。
1.肺尘埃沉着病(尘肺):有相关职业史,常有气促、胸闷、胸痛,且进行性加重;查体可有支气管移位和叩诊浊音;肺功能检查早期示限制性通气功能障碍,后期同时有弥散功能障碍。X线胸片表现为结节阴影、网状阴影和/或大片融合病灶,其次为肺门改变、肺纹理改变和胸膜改变。本例患者粉尘吸入史短,肺内未见典型矽结节改变,故不支持尘肺诊断。
2.血行播散型肺结核(粟粒性肺结核):多有午后低热、夜间盗汗,可有咳嗽、咯血伴消瘦,有时伴有肺外结核症状。双肺CT、痰找抗酸杆菌等检查可帮助鉴别,诊断困难时,可行诊断性治疗。本例患者无典型结核中毒症状,胸部CT未见粟粒样结节影,故可排除粟粒性肺结核。
3.过敏性肺炎:是易感个体反复吸入有机粉尘抗原后诱发的一种主要通过细胞免疫和体液免疫反应介导的肺部变态反应性疾病。一般状态下,患者在职业或家居环境接触抗原后4~8小时出现畏寒发热、全身不适,伴胸闷、呼吸困难和咳嗽,脱离抗原接触24~48小时可恢复。根据明确的抗原接触史,典型的临床症状发作特点,胸部HRCT见细支气管中心结节、斑片磨玻璃影或实变,气管陷闭形成马赛克征象等特征性表现,BALF检查显示淋巴细胞明显增加,可以做出诊断。
4.嗜酸性粒细胞性肺炎:是一种以肺部嗜酸性粒细胞浸润伴有或不伴有外周血嗜酸性粒细胞增多为特征的临床综合征,常见于中年女性,通常于数周或数月内出现呼吸困难、咳嗽、发热、盗汗、体重减轻和喘鸣,呈现急性、亚急性或慢性病程。X线胸片的典型表现为肺外带致密肺泡渗出影,中心带清晰,这种表现称为肺水肿反转形状,而且渗出性病变多位于上叶。80%患者出现外周血嗜酸性粒细胞增多,血清IgE增高也常见,BALF嗜酸性粒细胞>40%。本病例应注意与之鉴别。
5.肺泡蛋白沉积症(PAP):以肺泡腔内积聚大量表面活性物质为特征,好发年龄为30~50岁,男女患病比例为(2~4)∶1,至今病因不明。PAP可分为先天性、免疫性和继发性3种类型。大多数先天性PAP在婴幼儿或儿童期发病,也可在成年以后出现症状。免疫性PAP最为常见,占90%以上,是自身免疫性疾病,主要是由于体内存在的抗粒细胞-巨噬细胞集落刺激因子(GM-CSF)自身抗体导致肺泡巨噬细胞对表面活性物质清除障碍所致。继发性PAP与许多基础疾病有关,可伴发PAP的疾病有:①肺部感染,如分枝杆菌病、肺孢子菌肺炎和巨细胞病毒感染等;②继发于恶性肿瘤或免疫功能严重低下的疾病,如淋巴瘤、白血病等;③吸入矿物质或化学物质(二氧化硅铝粉等)。典型PAP患者X线胸片显示两肺弥漫性高密度影改变,分布于肺门周围,形成蝶形图案,并且双肺广泛渗出病变与无明显临床症状相分离。PAP患者胸部HRCT特征性表现:①磨玻璃影与正常肺组织截然分开,形成地图样病灶;②小叶间隔和小叶内间隔增厚,形成多边形或不规则铺路石样图案。PAP特征性病理生理改变是肺内分流导致严重低氧血症。BAL回收液呈奶白色,稠厚且不透明,静置后沉淀分层。BALF细胞或TBLB组织PAS染色阳性和阿辛蓝染色阴性可以证实诊断。本病例临床表现为咳嗽、咳痰、胸闷、气促、低氧血症,影像学检查见双肺弥漫性渗出性病灶,有煤矿工作史,应高度怀疑肺泡蛋白沉积症。
二、诊治过程及确诊
根据上述分析,本病例可能的诊断为肺泡蛋白沉积症,目前需要积极完善相关检查,如支气管肺泡灌洗、经皮穿刺肺活检等,以明确病因。
(一)临床信息
【实验室检查】
血常规:WBC 16.86×109/L,N% 80.3%,ESR 19mm/1h。
血生化:TP 61.33g/L,ALB 34.96g/L,LDH 254IU/L ;CRP 136.84mg/L。
乙肝表面抗原、梅毒螺旋体抗体、丙肝病毒抗体、人类免疫缺陷病毒抗体均为阴性。
肿瘤标志物检查:CEA 19.1ng/ml,NSE 21.6ng/ml,CYFRA21-1 21.6ng/ml,CA50 15.33IU/ml。
血气分析:pH 7.488,PaO2 58.3mmHg,PaCO2 35.8mmHg,SaO2 92.3%。
ANCA-MPO、ANCA-PR3和其他自身抗体均阴性;ENA多肽抗体均为阴性;补体C3、C4正常;呼吸道多种病毒(呼吸道合胞病毒、腺病毒、流行性感冒病毒等)抗原检测阴性。
【其他辅助检查】
胸部CT:双肺可见弥漫性网格状密度增高影,支气管壁增厚;右下肺可见团片状密度增高影,边缘不清,密度不均,有小空洞形成;双侧胸膜肥厚粘连,气管、支气管通畅,纵隔淋巴结增大(图1)。
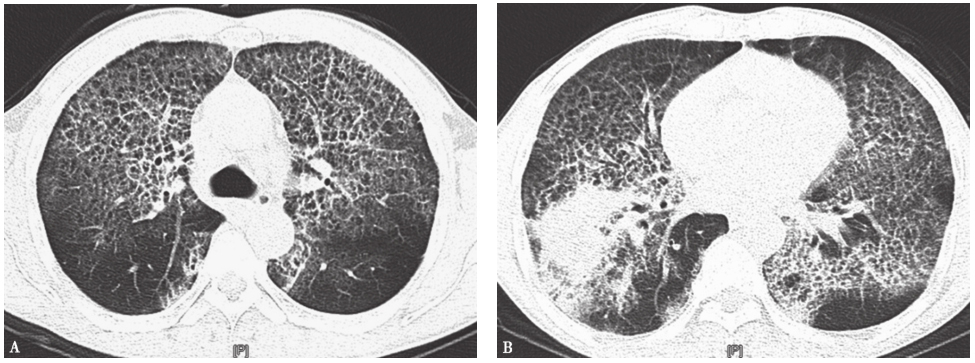
图1入院第2天胸部CT表现
胸部CT可见双肺弥漫性网格状密度增高影(A),右下肺团片状密度增高影(B)
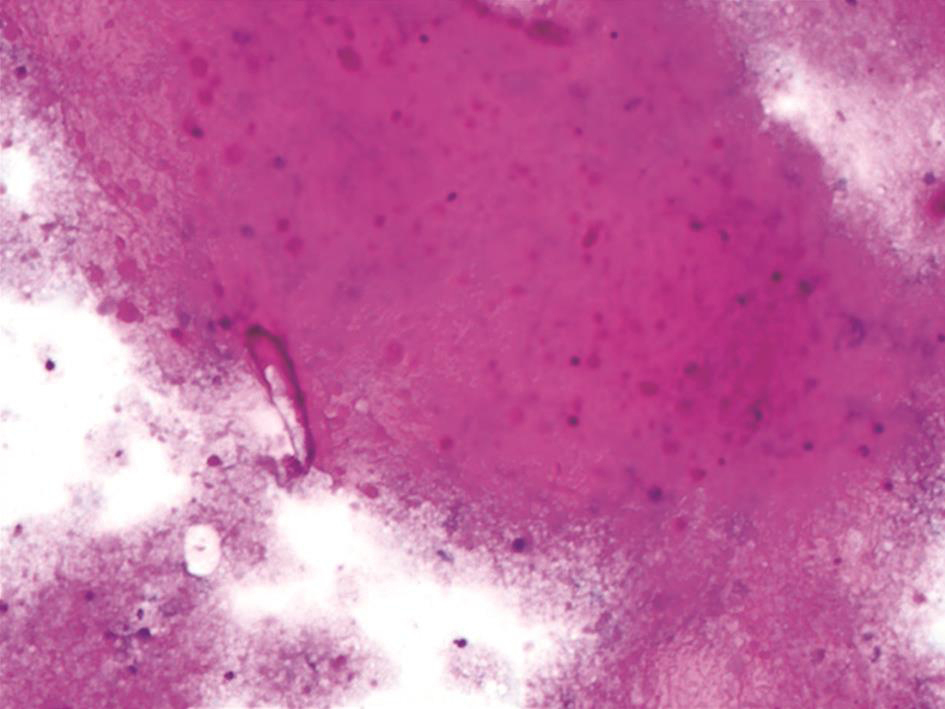
支气管镜检查(入院后第3天):见支气管腔内较多黄色黏稠分泌物,予吸引治疗;各叶段管腔通畅,腔内未见出血、狭窄、新生物(图2);于右上叶行生理盐水灌洗,灌洗液呈浑浊牛奶样改变;支气管镜下右下叶基底段刷检未见癌细胞,刷检找抗酸杆菌阴性;支气管肺泡灌洗液PAS染色阳性(图3)。
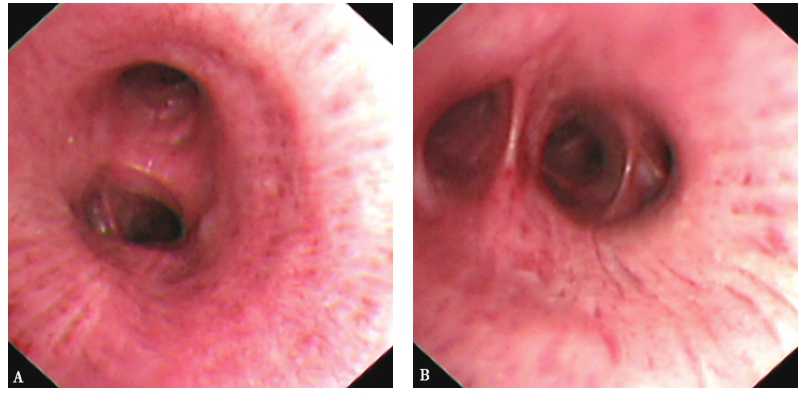
图2支气管镜检查镜下表现
镜下见双侧支气管黏膜充血,管腔通畅
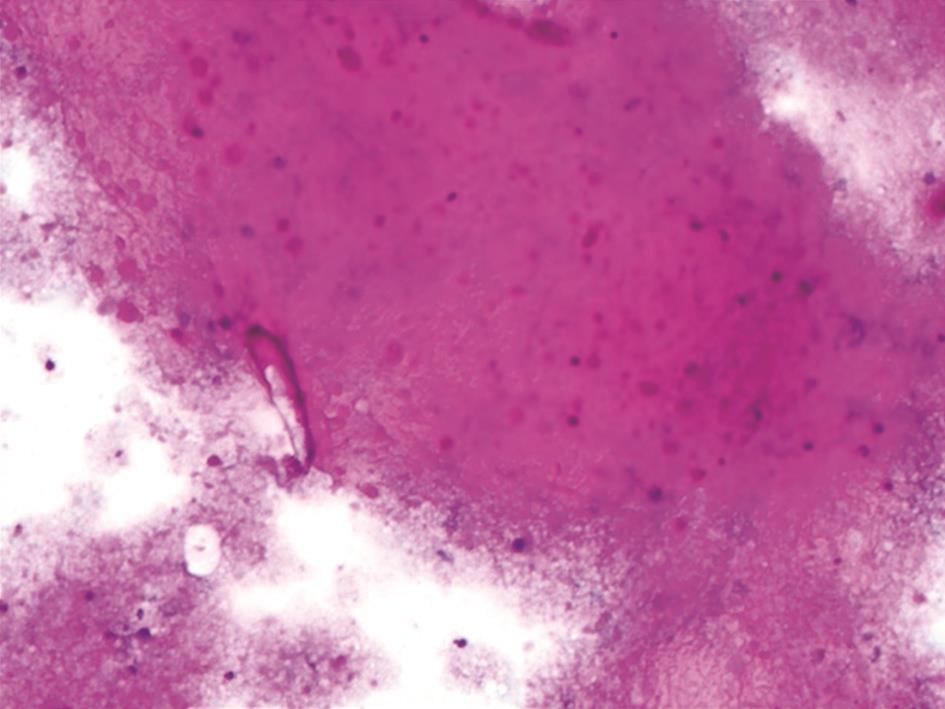
图3支气管肺泡灌洗液PAS染色阳性(400×)
CT引导下经皮穿刺肺活检病理检查(入院后第4天):送检右下肺穿刺活检组织,显微镜下见肺泡间隔增宽、纤维化,有慢性炎症细胞浸润及炭末沉着,肺泡腔内见较多吞噬细胞,未见其他异常表现(图4)。
肺功能检查提示限制性通气功能障碍。
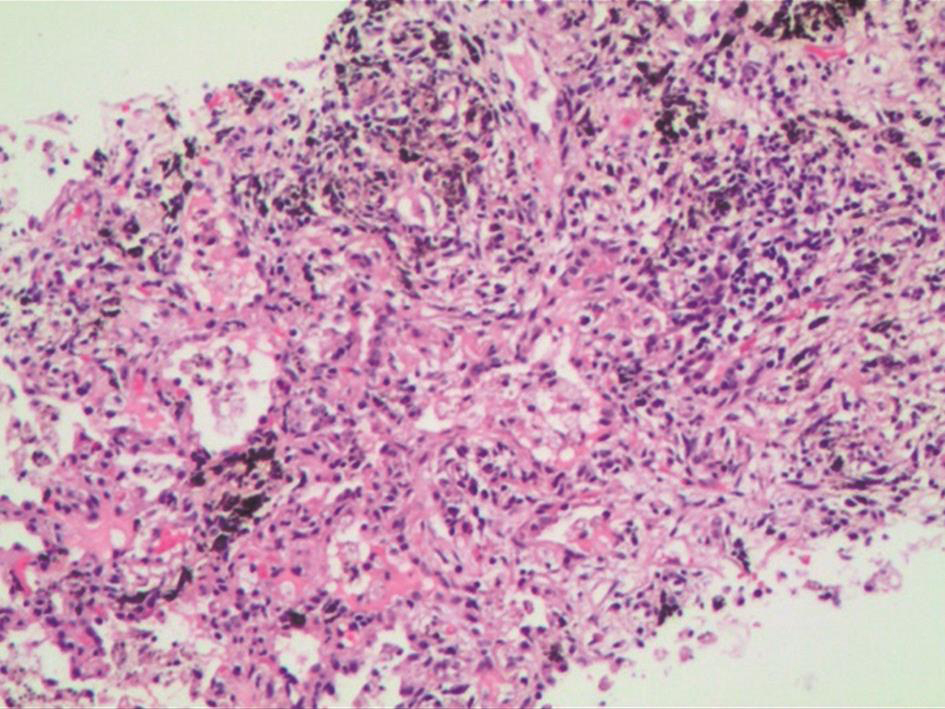
图4右下肺穿刺活检组织病理表现(HE染色,200×)
最后诊断:肺泡蛋白沉积症。
入院后第2周和第3周分别于全麻下行大容量左、右肺灌洗术,灌洗液为牛奶状浑浊液体,沉淀后瓶底见较多沉淀物,漂浮有少量絮状物(图5)。

图5支气管肺泡灌洗液
术后,给予减轻肺水肿(呋塞米)、吸氧、抗感染、舒张支气管、祛痰及无创机械通气等治疗,患者感胸闷气促等症状明显缓解。1个月后复查CT提示双肺病灶较前吸收,右下肺大片实变影较前缩小(图6)。患者病情好转出院后,采取吸入GM-CSF治疗,定期随访,状态良好。
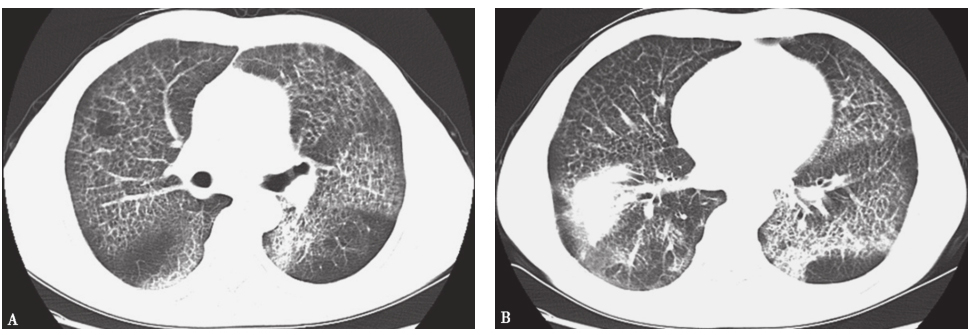
图6入院1个月后胸部CT表现
(二)临床思辨
患者就诊长达8个月,曾经接受抗感染和激素治疗,效果不佳,经过系列检查,在排除感染性疾病和风湿免疫病所致肺损伤后,确诊为PAP。
PAP可分为先天性、免疫性和继发性3种类型。大多数先天性肺PAP在婴幼儿或儿童期发病,但也可在成年以后出现症状。PAP大多数为隐匿起病,10%~30%诊断时无症状。常见症状是呼吸困难伴咳嗽,偶有咳痰,其中呼吸困难最常见,约占54.3%。
PAP的病因仍不十分明确,一般认为它是一种自身免疫性疾病,主要是由于体内存在的抗粒细胞-巨噬细胞集落刺激因子(GM-CSF)自身抗体导致肺泡巨噬细胞对表面活性物质清除障碍所致。电镜观察发现,肺泡蛋白沉积物和全肺灌洗物在结构上与由Ⅱ型肺泡上皮细胞分泌的含有层状体的肺泡表面活性物质非常相似,提示肺泡蛋白沉积物可能与肺泡表面活性物质代谢障碍有关。
对于PAP,目前尚无特效治疗方法,针对合并感染者的抗感染治疗能不同程度地改善肺功能并缓解症状。部分患者可以自行缓解,但机制不明确。
全肺灌洗:对于有明显呼吸功能障碍的患者,全肺灌洗(whole lung lavage,WLL)是首选和有效的治疗方法,50%患者可缓解症状。但有部分患者即便反复行全肺灌洗术,病情也可能不断进展。所以,对于症状较重(PaO2<60mmHg)的患者,首选肺灌洗治疗以改善症状,若病情进展快,可反复进行肺灌洗;而对于症状较轻、日常活动轻度或基本不受限的患者,可予以对症支持治疗并密切随访,以减少肺灌洗术的次数和相应的风险。
GM-CSF替代治疗:虽然目前全肺灌洗术仍是PAP的首选治疗方法,但是该治疗方法并不能针对病因。近年来,国内外学者尝试使用GM-CSF替代疗法治疗PAP,效果良好。皮下注射重组GM-CSF对特发性PAP有一定疗效,但易发生外周白细胞增多。雾化吸入重组GM-CSF局部治疗PAP的有效率可达91.7%,且更安全,全身不良反应小。
抗CD20抗体(利妥昔单抗)治疗:抗CD20抗体是针对自身免疫性PAP的另一种有前途的治疗方法。研究显示,这种人鼠嵌合的单克隆抗体(利妥昔单抗)可以直接针对B淋巴细胞特异性抗原CD20,通过减少B细胞表达CD20,抑制浆细胞产生GM-CSF抗体,从而治疗免疫性PAP。Malur等观察了10例接受CD20抗体(利妥昔单抗)治疗的PAP患者,结果显示利妥昔单抗可减少支气管肺泡灌洗液中GM-CSF抗体水平,完成全程试验的9例患者中7例患者经动脉血氧检查证实有临床改善。因此,PAP治疗策略是在支气管肺泡灌洗治疗基础上,序贯吸入GM-CSF,若治疗失败可考虑应用CD20抗体(利妥昔单抗)治疗。
其他治疗还有血浆置换、骨髓移植、自体造血干细胞移植、基因治疗、机械通气等。对于继发性PAP,还应针对原发病治疗。外科肺移植因对PAP的疗效不确定且创伤和风险极大,不推荐开展。
精要回顾与启示
咳嗽、咳痰、气短是弥漫性间质性肺疾病的常见临床表现,而胸部CT呈弥漫性渗出性病灶亦可见于多种弥漫性间质性肺疾病。肺泡蛋白沉积症在临床上并不少见,有多种因素可导致PAP(诸如吸入物及粉尘等明确诱因或免疫相关性),影像学表现为地图征和铺路石征,无明显临床症状,支气管肺泡灌洗液呈牛奶样外观。掌握PAP的特征对及早明确诊断、及时采取相应治疗至关重要。
知识来源
人卫知识数字服务体系
- 评价此内容
- 我要打分
近期推荐
热门关键词
最新会议
- 2013循证医学和实效研究方法学研讨会
- 欧洲心脏病学会年会
- 世界帕金森病和相关疾病2013年会议
- 英国介入放射学学会2013年第25届年会
- 美国血液学会2013年年会
- 美国癫痫学会2013年第67届年会
- 肥胖学会 2013年年会
- 2013年第9届欧洲抗体会议
- 国际精神病学协会 2013年会议
- 妇科肿瘤2013年第18届大会
- 国际创伤压力研究学会2013年第29届…
- 2013年第4届亚太地区骨质疏松症会议
- 皮肤病协会国际2013年会议
- 世界糖尿病2013年大会
- 2013年国际成瘾性药年会
- 彭晓霞---诊断试验的Meta分析
- 武姗姗---累积Meta分析和TSA分析
- 孙凤---Network Meta分析
- 杨智荣---Cochrane综述实战经验分享
- 杨祖耀---疾病频率资料的Meta分析
合作伙伴
Copyright g-medon.com All Rights Reserved 环球医学资讯 未经授权请勿转载!
网络实名:环球医学:京ICP备08004413号-2
关于我们|
我们的服务|版权及责任声明|联系我们
互联网药品信息服务资格证书(京)-经营性-2017-0027
互联网医疗保健信息服务复核同意书 京卫计网审[2015]第0344号


 会员登录
会员登录

