老爷爷体检发现腹腔肿块 确诊为?怎么治?
80岁男性,因“体检发现腹腔肿块2周”入院,如何诊治?
【病例摘要】
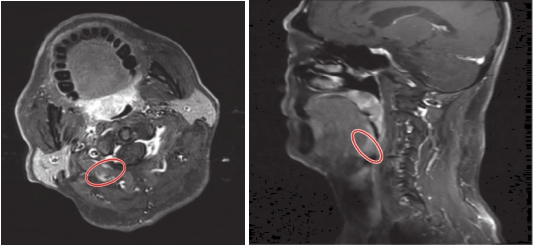
患者,男性,80岁,于2014年6月因“体检发现腹腔肿块2周”入院。行腹部CT示:胃小弯近贲门部肿物,考虑胃壁来源间质瘤可能性大。肝S2低密度病灶,考虑肝囊肿可能性大。右下肺及左上肺尖少许纤维增殖灶。纵隔小淋巴结、双侧腹股沟小淋巴结肿大(图1)。胃镜示:贲门胃底见溃疡型肿物,大小约3.5cm×3.0cm,溃疡底部覆盖污苔,边缘黏膜不规则隆起,局部僵硬,边界不清,质地脆,易出血(图2)。活检病理提示:中分化腺癌。门诊以“食管胃结合部癌(Ⅲ型)”收入。
既往史及家族史
既往体健,否认药物过敏史;父母健在,家族中无类似病史。
体格检查
生命体征平稳,皮肤黏膜无黄染、无苍白。腹部平坦,无压痛及反跳痛,未见胃肠型及蠕动波。肠鸣音正常。
图1 腹部CT
图2 胃镜检查
辅助检查
血常规:白细胞24.5×109/L↑,血红蛋白92g/L↓,血小板90.9×109/L↓。
肿瘤标记物:CEA、CA199正常;CA72-4 5.63U/ml↑。
生化、凝血功能正常。
心脏彩超、肺功能无明显异常。
初步诊断
1. 食管胃结合部癌(Ⅲ型)
2. 白细胞增高原因待查
【治疗过程】
(一)病例分析
患者为老年男性,以“体检发现腹腔肿块2周”就诊。目前初步诊断:①食管胃结合部癌(Ⅲ型);②白细胞增高原因待查。关于血象增高,请血液科会诊意见:考虑肿瘤引起的血象异常,慢性粒细胞白血病暂排除,建议骨髓穿刺活检。骨髓穿刺活检病理回复:①骨髓增生活跃,其中粒细胞系统有轻度核左移现象;②涂片未见恶性肿瘤细胞。经多学科讨论认为:患者胃癌诊断明确,无远处转移,局部病灶切除可能性较大,白细胞升高可能是胃癌肿瘤引起,无明显手术禁忌证,决定手术治疗。
(二)治疗方案
于2013年7月12日全麻下行“胃癌根治术(全胃切除+脾切除+D2淋巴结清扫+ Roux-en-Y重建)”。术中探查情况:腹盆腔、肝脏未及转移结节,原发肿瘤位于胃底贲门处,约7cm×6cm大小,向腹膜后侵犯,与脾门关系紧密,未侵犯胰腺、结肠、肝脏。术后标本解剖:胃底贲门溃疡型肿物,约4cm×3cm大小(图3),肿物旁贲门右可及一个与肿物不相连的肿块(肿大淋巴结?)(图4),约6cm×7cm大小。
图3 胃底贲门溃疡型肿物
图4 贲门右不相连的肿物
(三)术后病理及基因检测
术后病理:大体:近贲门处菜花样肿物,约3.5cm×3cm×1cm大小,灰白、质硬;胃肿物旁及不相连的可疑肿大淋巴结(贲门右)约7cm×4cm×6cm大小,切面灰白、质硬,有部分包膜。镜下:胃中至低分化腺癌,Lauren分型为肠型,浸润至胃壁浅肌层,未见明显脉管内癌栓及神经束侵犯;网膜组织及脾组织未见癌。淋巴结1/45(+)。免疫组织化学染色:VEGF(+),Her-2(3+),CEA(+),CD56(+),Syn(-),CgA(-),NSE(-),Ki-67(Li:15%)。
可疑(贲门右)淋巴结:镜下见梭形细胞束状或漩涡状排列,细胞轻度异型,可见核分裂象(3个/50HPF),未见明显坏死及囊性变,结合免疫组织化学染色结果,病变诊断为胃肠间质瘤。免疫组织化学染色:CD117(+),CD34(+),DOG-1(+),S100(-),desmin(-),HHF35(-),Ki-67(Li:>5%)。
【预后】
术后患者恢复良好,血白细胞从42×109/L(手术当天)降至36×109/L,术后第9天中性粒细胞百分比61.89%,在正常范围内。患者无发热、咳嗽、咳痰、腹痛等感染表现,请血液科会诊后,予观察处理。术后第9天予拆线出院。
【经验与体会】
(一)胃肠道癌合并胃肠间质瘤
据报道,大约有20%~30%的正常人有小(<2cm)的GIST,这些小GIST很多是在一些因其他原因尸检的时候发现的,但是一直都没有长大。事实上,胃肠道癌合并GIST也常见,经常在胃癌手术切下来的标本中可见小GIST,这些小GIST通常都是极低危的,并不需要特别处理。然而,胃肠道癌合并中高危GIST不太常见,本病例便是其中一例。
(二)胃肠道癌合并胃肠间质瘤的术式该怎么选择?
在确认胃肠道癌合并胃肠间质瘤可手术的患者中,首先需要明确肿瘤的部位、大小以及切缘设计。总体上,进展期胃癌需要满足足够切缘以及淋巴结清扫范围,而GIST的手术并没有对切缘多少作要求且不需淋巴结清扫,但是必须保证肿瘤完整切除达到R0切除。因此,手术切除范围可在满足胃癌切除范围上,尽量R0切除GIST。
(三)该如何进行术后辅助治疗?
这例患者胃癌是局部进展期(pT2N1M0,ⅡA期),胃肠间质瘤NIH危险度分级为中危,AFIP复发风险为:3.6%。理论上,该患者无论是胃癌还是GIST均需要进行辅助治疗,可考虑单药替吉奥辅助治疗胃癌同期予以伊马替尼400mg/d治疗,或者在替吉奥辅助治疗胃癌结束后再给予伊马替尼治疗。但考虑该患者年龄已77岁,且胃癌及胃肠间质瘤分期均较早,手术切除后总体预后良好,复发风险不算太高,因此和患者及家属沟通后,放弃辅助治疗,建议定期复查和密切随访。
(撰稿人:邱海波)
【专家点评】
李乐平
教授,主任医师,博士研究生导师,泰山学者
山东省立医院副院长、普外科主任、胃肠外科主任
中华医学会外科学分会委员
中国医师协会外科医师分会常务委员
中国医师协会外科医师分会胃肠道间质瘤诊疗专业委员会副主任委员
山东省医学会外科学分会委员会主任委员
合并其他肿瘤的GIST患者约占全部患者的20%,其中有约25%为消化道恶性肿瘤,最常见的为结直肠与食管胃底结合部的恶性肿瘤,并发的大多数为小的极低危的GIST,本例报道了贲门恶性肿瘤合并中危GIST。术前及术后的血常规显示WBC明显升高,考虑胃癌引起可能,但应进一步持续观察以排除血液系统疾病。尤其是肿瘤切除术后WBC仍然较高时,应特别注意。
合并消化道恶性肿瘤的GIST接受辅助治疗的比例较低,一方面是因为此类患者多数肿瘤较小,复发危险度分级较低,另一方面也因为此类患者接受辅助治疗的依从性较差。本例患者为进展期的胃癌合并中危GIST,《中国胃肠间质瘤诊断治疗共识(2017年版)》推荐中危胃GIST患者术后接受一年的伊马替尼靶向治疗,而进展期胃癌常见的术后化疗方案以铂类或氟尿嘧啶为基础的化疗方案为主,两类疾病的系统治疗重合度较低。在制订此类患者的辅助治疗方案时,考虑GIST与伴发肿瘤的治疗指南的同时,更要考虑辅助化疗与靶向治疗对患者一般情况的影响以及药物相互作用,在延长患者生存期的同时保证患者的生存质量。
【参考文献】
[1] 鲁常青, 沈云志, 田波. 胃肠道间质肿瘤伴发消化道癌 [J] . 中华消化内镜杂志, 2004, 21 (6) : 371-373.
[2] LIU Z, LIU S, ZHENG G, et al. Clinicopathological features and prognosis of coexistence of gastric gastrointestinal stromal tumor and gastric cancer [J] .Medicine (Baltimore) , 2016, 95 (45) : e5373.
[3] CONRAD C, NEDELCU M, OGISO S, et al.Laparoscopic intragastric surgery for early gastric cancer and gastrointestinal stromal tumors [J] . Ann Surg Oncol, 2014, 21 (8) : 2620.
[4] LIU S, LIU H, DONG Y, et al. Gastric carcinoma with a gastrointestinal stromal tumor-A case report and literature review [J] . Med Sci (Paris) , 2018, 34: 15-19.
[5] LIN M, LIN J X, HUANG C M, et al. Prognostic analysis of gastric gastrointestinal stromal tumor with synchronous gastric cancer [J] . World J Surg Oncol, 2014, 12: 25.
(环球医学编辑:常路)
来源:《胃肠间质瘤典型病例诊治与解析》
作者:陶凯雄 曹晖
页码:181-186
出版:人民卫生出版社
- 评价此内容
- 我要打分
近期推荐
热点文章
热门关键词
合作伙伴
Copyright g-medon.com All Rights Reserved 环球医学资讯 未经授权请勿转载!
网络实名:环球医学:京ICP备08004413号-2
关于我们|
我们的服务|版权及责任声明|联系我们
互联网药品信息服务资格证书(京)-经营性-2017-0027
互联网医疗保健信息服务复核同意书 京卫计网审[2015]第0344号


 会员登录
会员登录

